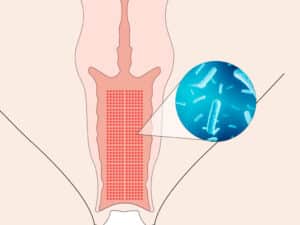
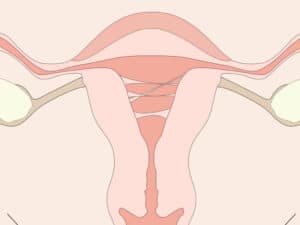
El Síndrome de Asherman (AS) es una afección a menudo vinculada a traumas que afecta al endometrio, la capa basal del útero. Este síndrome se manifiesta cuando el endometrio sufre daño, ya sea por trauma físico o después de un legrado. Estas situaciones desencadenan inflamación, predisponiendo la formación de bandas adhesivas de un lado de la cavidad uterina a otro. A este proceso le sigue la deposición descontrolada de la matriz extracelular y colágenos fibrilares. El factor de crecimiento transformador beta (TGF) desempeña un papel central en la fibrogénesis, encontrándose en mayores cantidades en el endometrio dañado en comparación con el endometrio normal. Factores fibrosantes como TGF beta 1, alfa SMA, CTGF y colágeno I y III son cruciales para el desarrollo de adherencias intrauterinas, alterando así el entorno uterino y reduciendo la capacidad regenerativa de las células madre mesenquimales endometriales.
Esta condición a menudo conduce a problemas de fertilidad, abortos habituales, irregularidades menstruales, dolor crónico en la pelvis y, durante el embarazo, posiciones irregulares de la placenta, como la placenta previa o accreta. Los principales factores de riesgo son legrados, especialmente después de un aborto, y procedimientos quirúrgicos como la miomectomía, la histeroscopia y la cesárea.
Diagnóstico y tratamiento convencional
El diagnóstico estándar de AS se realiza mediante histeroscopia, siendo este el método de elección según la Sociedad Europea de Endoscopia Ginecológica. La prevalencia en mujeres infértiles varía entre el 2% y el 22%. El tratamiento incluye la lisis de adherencias por histeroscopia, seguida de terapia con progesterona y estrógeno para estimular la regeneración endometrial y el uso de barreras para prevenir la re-adhesión.
A veces, AS puede no diagnosticarse mediante procedimientos rutinarios como la ecografía debido a su falta de sensibilidad. La delgadez del endometrio está presente en un 13% de mujeres con pérdida de embarazo en el primer trimestre y en el 30% de mujeres sometidas a legrados por abortos tardíos.
Tratamiento con células madre
En la búsqueda de alternativas terapéuticas, se ha explorado el potencial de las células madre mesenquimales (MSC). Investigaciones recientes han demostrado que la terapia con MSC, mediante la secreción de factores de crecimiento y citoquinas, puede reducir la inflamación y promover la regeneración del tejido. Un estudio realizado por Zhang et al. evaluó la eficacia de la terapia con células madre del cordón umbilical (CS/UC-MSC) para regenerar el endometrio en mujeres con AS. Después del trasplante, se observó un aumento significativo en el grosor del endometrio, y varias mujeres lograron embarazos exitosos mediante transferencia de embriones congelados.
En otro estudio de Jichun Tan I et al., se analizó el efecto de las MSC obtenidas de la sangre menstrual en la regeneración endometrial en mujeres con AS. Los resultados fueron prometedores, con significativa proliferación del endometrio en todas las pacientes, algunas alcanzando un grosor adecuado para la transferencia de embriones.
Un estudio liderado por Hailan Ma et al. evaluó los efectos del trasplante intrauterino de MSC de la sangre menstrual en mujeres con AS refractario. Después del trasplante, se observó una mejora significativa en el grosor endometrial y, lo más alentador, cinco pacientes lograron embarazos exitosos.
En resumen, los avances en el tratamiento del Síndrome de Asherman con células madre mesenquimales abren nuevas perspectivas para las mujeres que enfrentan esta condición, ofreciendo esperanza y oportunidades renovadas para la fertilidad y la maternidad. Estos descubrimientos marcan un hito en la búsqueda de soluciones efectivas y menos invasivas para abordar este desafío ginecológico.
Fuente:
Ivkošić, I. E., Fureš, R., Ćosić, V., Mikelin, N., Bulić, L., Dobranić, D., Brlek, P., & Primorac, D. (2023). Unlocking the Potential of Mesenchymal Stem Cells in Gynecology: Where Are We Now? Journal Of Personalized Medicine, 13(8), 1253. https://doi.org/10.3390/jpm13081253

Aprende desde cero a realizar procedimientos de ginecología estética funcional
Curso exclusivo para especialistas
Referencias:
- Benor, A.; Gay, S.; DeCherney, A. An update on stem cell therapy for Asherman syndrome. J. Assist. Reprod. Genet. 2020, 37, 1511–1529. [Google Scholar] [CrossRef]
- Hu, J.; Zeng, B.; Jiang, X.; Hu, L.; Meng, Y.; Zhu, Y.; Mao, M. The expression of marker for endometrial stem cell and fibrosis was increased in intrauterine adhesious. Int. J. Clin. Exp. Pathol. 2015, 8, 1525–1534. [Google Scholar]
- Tan, J.; Li, P.; Wang, Q.; Li, Y.; Li, X.; Zhao, D.; Xu, X.; Kong, L. Autologous menstrual blood-derived stromal cells transplantation for severe Asherman’s syndrome. Hum. Reprod. 2016, 31, 2723–2729. [Google Scholar] [CrossRef] [Green Version]
- Smikle, C.; Yarrarapu, S.N.S.; Khetarpal, S. Asherman Sindrome StatPearls; StatPearls Publishing: Treasure Island, FL, USA, 2021. Available online: www.ncbi.nlm.nih.gov/books/NBK448088 (accessed on 30 March 2023).
- Zhang, Y.; Shi, L.; Lin, X.; Zhou, F.; Xin, L.; Xu, W.; Yu, H.; Li, J.; Pan, M.; Pan, Y.; et al. Unresponsive thin endometrium caused by Asherman syndrome treated with umbilical cord mesenchymal stem cells on collagen scaffolds: A pilot study. Stem Cell Res. Ther. 2021, 12, 420. [Google Scholar] [CrossRef]
- Zhao, Y.; Luo, Q.; Zhang, X.; Qin, Y.; Hao, J.; Kong, D.; Wang, H.; Li, G.; Gu, X.; Wang, H. Clinical Efficacy and Safety of Stem Cell-Based Therapy in Treating Asherman Syndrome: A System Review and Meta-Analysis. Stem Cells Int. 2020, 2020, 8820538. [Google Scholar] [CrossRef] [PubMed]
- Ma, H.; Liu, M.; Li, Y.; Wang, W.; Yang, K.; Lu, L.; He, M.; Deng, T.; Li, M.; Wu, D. Intrauterine transplantation of autologous menstrual blood stem cells increases endometrial thickness and pregnancy potential in patients with refractory intrauterine adhesion. J. Obstet. Gynaecol. Res. 2020, 46, 2347–2355. [Google Scholar] [CrossRef]